Les fondamentaux des liaisons hydrogène et de la tension superficielle de l’eau
Les liaisons hydrogène jouent un rôle essentiel dans la chimie de l’eau, influençant non seulement ses propriétés physico-chimiques, mais aussi sa dynamique. Ces liaisons, qui se forment entre les molécules d’eau, sont responsables de l’anomalie de la tension superficielle de ce liquide. Cette tension est définie comme la force qui agit à la surface d’un liquide, créant un film élastique qui permet à des insectes aquatiques, comme les striders, de marcher sur l’eau sans y couler.
Pour comprendre cette anomalie, il est crucial de se pencher sur la nature même des liaisons hydrogène. Ce sont des interactions spécifiques qui se produisent entre un atome d’hydrogène, lié de manière covalente à un atome électronégatif (comme l’oxygène dans le cas de l’eau), et un autre atome électronégatif. Ces liaisons sont simultanément plus faibles que les liaisons covalentes, mais elles apportent une robustesse suffisante pour influencer la structure moléculaire et la dynamique du liquide.
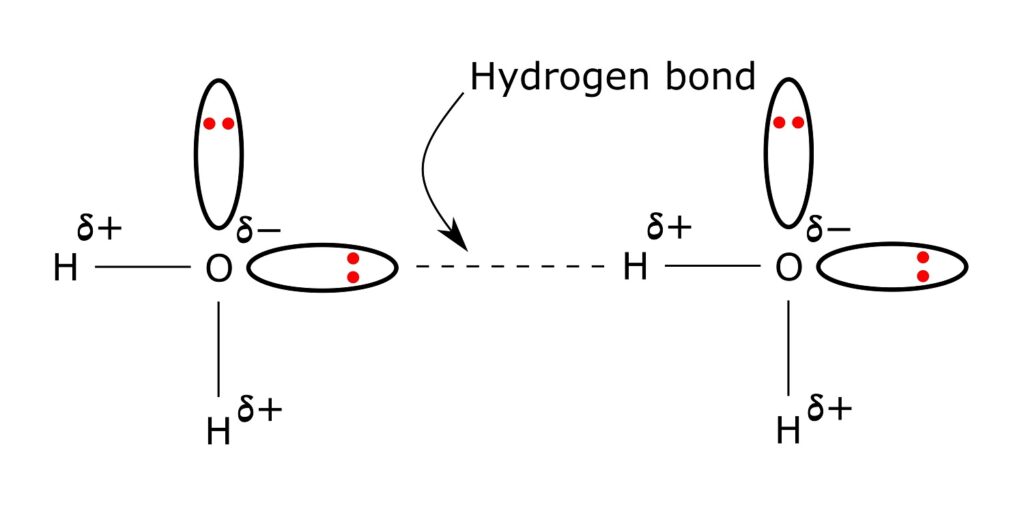
Le réseau de liaisons hydrogène dans l’eau génère une organisation complexe des molécules. À température ambiante, une molécule d’eau forme en moyenne quatre liaisons hydrogène avec ses voisines, mais à la surface, cette capacité est réduite, ce qui engendre une différence de pression qui contribue à la tension superficielle élevée.
Il est fascinant de noter que la tension superficielle de l’eau est d’environ 72 mN/m, ce qui est supérieur à celle de nombreux autres liquides organiques. Ce phénomène est attribué au coût énergétique lié à la rupture des liaisons hydrogène lorsque la surface est formée. La grande force des liaisons hydrogène crée un réseau cohésif qui minimise l’interaction de l’eau avec l’environnement. Ainsi, cette anomalie de la tension superficielle peut être directement liée aux dynamiques des liaisons hydrogène dans l’eau.
La compréhension de cette dynamique est cruciale pour diverses applications pratiques, qu’il s’agisse de la biologie ou de l’ingénierie des matériaux. Par exemple, la tension superficielle de l’eau influence les processus de filtrage et de purification dans les systèmes de traitement de l’eau. En outre, les liaisons hydrogène jouent un rôle fondamental dans la solvatation des ions, qui est essentielle pour de nombreuses réactions chimiques.
| Propriété | Détails |
|---|---|
| Liaison hydrogène | Interaction entre un hydrogène et un atome électronégatif |
| Tension superficielle de l’eau | Environ 72 mN/m à température ambiante |
| Rôle dans la biologie | Influence sur les protéines et les membranes cellulaires |
La synergie entre ces liaisons et la nature du liquide lui-même est un domaine d’étude d’un grand intérêt scientifique. En examinant plus en profondeur les mécanismes à l’œuvre, nous pouvons également éclairer des domaines variés comme la dynamique des fluides en milieu biologique et les technologies de conservation de l’eau.
Les structures moléculaires complexes de l’eau et leur impact sur la tension superficielle
L’eau, bien que moléculairement simple, présente une complexité fascinante en raison de la configuration spatiale de ses atomes. Chaque molécule d’eau adopte une structure en forme de « V » en raison de l’angle de 104,5° entre les liaisons O-H. Cette géométrie est cruciale pour la formation de réseaux d’hydrogène qui, par leur nature anisotrope, influencent la tension superficielle.
Lorsque les molécules d’eau interagissent entre elles, surtout à la surface, elles montrent des comportements de compétition entre différents arrangements structuraux : l’état Tetraédrique (S-state) et l’état désordonné (ρ-state). Dans l’état S-state, l’eau forme des liaisons hydrogène stabilisantes qui favorisent un agencement bien structuré, tandis que l’état ρ-state correspond à une orientation moléculaire plus aléatoire.
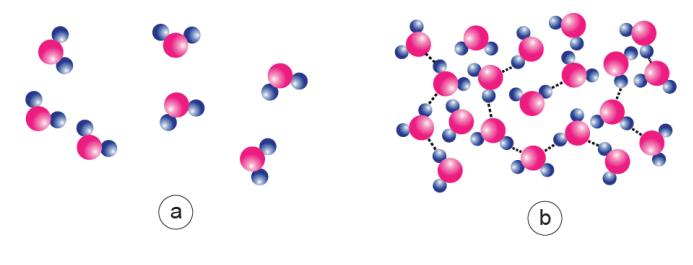
À température ambiante, la majorité des molécules d’eau se trouvent dans des arrangements de type ρ-state. Cependant, à des températures plus basses, un déplacement vers une plus forte proportion de l’état S-state se produit, entraînant une dynamique différente. Cette dynamique des structures moléculaires est à la racine de l’anomalie observée dans la tension superficielle de l’eau.
Ainsi, une compréhension des interactions intermoléculaires dans ces deux états peut nous éclairer sur la façon dont la tension superficielle varie avec la température. Des études ont montré que sous un refroidissement profond, le S-state devient de plus en plus prévalent, amplifiant la tension due à des interactions dipolaire-dipolaire renforcées.
| État moléculaire | Caractéristiques |
|---|---|
| S-state | Configuration organisée, maximalisation des liaisons hydrogène |
| ρ-state | Configuration désordonnée, moins de liaisons hydrogène |
| Température influence | Transition de l’état ρ vers l’état S à froid |
Cela souligne l’importance de la dynamique des liaisons hydrogène dans la modélisation des réseaux d’hydrogène de l’eau, car la structure et le comportement des molécules d’eau sont profondément imbriqués dans leurs propriétés essentielles. Ces insights sont précieux pour des applications allant de la climatologie à l’ingénierie chimique.
Les conséquences de la structure moléculaire sur les propriétés physiques et chimiques
La structure moléculaire de l’eau et sa capacité à former des liaisons hydrogène posent des bases solides pour une multitude de propriétés physico-chimiques. Ces liaisons déterminent non seulement la tension superficielle, mais influencent également des phénomènes tels que la solubilité, l’acidité, et même la conductivité électrique.
Le fait que l’eau soit un solvant polaire en fait un excellent choix pour des réactions chimiques dans la nature. Les ions et les molécules polaires s’associent facilement en raison de leur interaction avec les molécules d’eau, ce qui permet des processus exothermiques ou endothermiques de se produire plus facilement. Cette capacité à solubiliser des substances est le fruit de la dynamique complexe de ses interactions intermoléculaires.
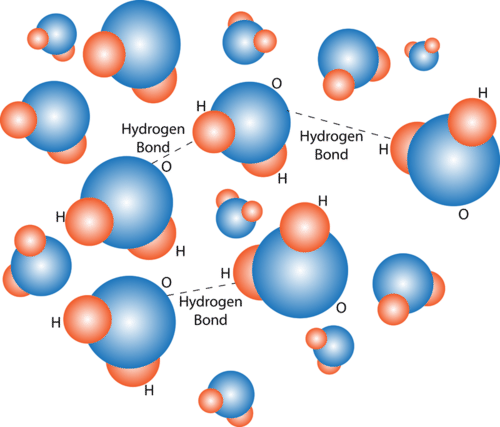
De plus, tout changement de température ou d’état physique modifie les liaisons hydrogène, ce qui entraîne des variations des propriétés de l’eau. Par exemple :
- À une température élevée, l’agitation des molécules d’eau peut rompre temporairement certaines liaisons, entraînant une baisse de la tension superficielle.
- En contrastant, à des températures basses, la solidité des liaisons hydrogène crée un environnement où la tension augmente, provoquant la formation de surfaces plus robustes.
- La présence de solutés dans l’eau modifie également les liaisons hydrogène, affectant la dynamique des interactions et, par conséquent, les propriétés du liquide lui-même.
| Propriété | Impact des liaisons hydrogène |
|---|---|
| Solubilité | Facilite la dissolution de composés ioniques et polaires |
| Acidité | Influence sur le pH et l’activité ionique dans l’eau |
| Conductivité | Réduction ou augmentation en fonction de la dynamique des liaisons |
Par conséquent, l’analyse des liaisons hydrogène permet de mieux comprendre non seulement la tension superficielle de l’eau, mais aussi d’autres aspects de sa chimie, comme sa réactivité dans différents environnements. L’importance de ces liaisons dans les processus biologiques et chimiques souligne qu’une telle compréhension pourrait avoir des implications à loin terme pour les applications environnementales et industrielles.
Influence de la température sur la dynamique des liaisons hydrogène et la tension superficielle
La relation entre température et dynamique des liaisons hydrogène est particulièrement fascinante. À mesure que la température diminue, les molécules d’eau se déplacent moins, permettant ainsi à la formation de liaisons hydrogène plus stabilisantes. C’est ici que la tension superficielle de l’eau présente une anomalie marquée, particulièrement dans le régime supercooled (sous-refroidi).
Dans les régimes entre 275 K et 250 K, des études ont montré une saturation des contributions de l’état ρ-state, tandis que l’état S-state, lui, commence à s’imposer, entrainant un comportement non linéaire croissant de la tension. Ceci se traduit par des observations remarquables où la tension superficielle augmente brutalement à des températures plus basses, une anomalie qui peut être expliquée par des interactions plus complexes des liaisons hydrogène.
Les conséquences de cette dynamique dépendent également de l’environnement local masqué :
- La formation de structures S-state à des températures plus basses diminue la flexibilité des liaisons, augmentant ainsi la résistance à la rupture.
- Cela favorise aussi l’émergence de motifs de structure comme Ice-0, qui sont essentiels pour la nucléation dans les milieux froids.
- Globalement, cette intensification des liaisons hydrogène à faible température influence les propriétés thermodynamiques et mécaniques de l’eau, ce qui est crucial pour l’évaluation de la physiologie des organismes aquatiques.
| Température (K) | Comportement de la tension superficielle (mN/m) |
|---|---|
| 300 | 72 (tension standard) |
| 275 | Transition vers une tension croissante |
| 250 | Augmentation rapide | En dessous de 250 | Augmentation significative de la tension superficielle |
Cette compréhension de la relation entre température, dynamique des liaisons hydrogène et tension superficielle de l’eau est essentielle pour mieux appréhender les phénomènes naturels, tels que la formation de gel de l’eau et la dynamique dans les écosystèmes aquatiques.
Applications pratiques basées sur les phénomènes de tension superficielle de l’eau
Les propriétés de la tension superficielle de l’eau, dérivées des liaisons hydrogène, ont des implications pratiques dans divers domaines allant de la biomédicine à l’ingénierie. Par exemple, la compréhension de ces propriétés est cruciale dans la conception de dispositifs qui exploitent les interactions liquides à des interfaces.
Dans le domaine biomédical, la tension superficielle de l’eau affecte directement l’absorption de substances par les cellules. Des études ont démontré que les cellules peuvent moduler leur comportement en réponse à la perturbation de cette tension, influençant ainsi la façon dont elles interagissent avec leur environnement liquide. Voici quelques applications notables :
- Utilisation en agriculture pour déterminer l’efficacité des pesticides et des engrais.
- Création de surfaces hydrophobes pour réduire l’adhérence des gouttes d’eau et améliorer le fonctionnement des appareils électroniques.
- Amélioration des techniques de nettoyage et désinfection basées sur des réactions chimiques favorisées par une tension superficielle élevée.
| Domaine d’application | Impact |
|---|---|
| Biomédical | Amélioration de l’absorption des médicaments |
| Agriculture | Optimisation de l’utilisation des nutriments |
| Ingénierie des matériaux | Création de surfaces anti-adhérentes |
Ces exemples illustrent clairement l’importance de la compréhension des ordres concurrents de liaisons hydrogène et de leur impact sur les propriétés physico-chimiques de l’eau. Le fait que ces propriétés soient liées à des phénomènes aussi variés renforce l’importance d’une recherche continue dans ce domaine fascinant de la science.
Source: www.nature.com
